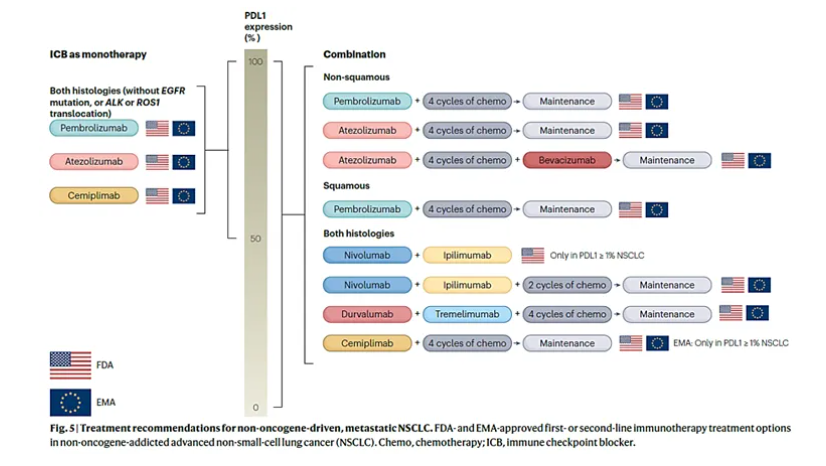
肺癌是全球发病率最高、致死率最高的癌种[1],其中,非小细胞肺癌(NSCLC)是最常见的肺癌亚型,占比约85% [2-3],又可分为鳞状与非鳞状癌(nsq-NSCLC),后者约占75%[4]。值得注意的是,大约三分之二的NSCLC患者在初诊时已处于晚期[5]。
NSCLC具有高度异质性,许多患者伴随多种驱动基因突变(如EGFR、ALK、ROS1、MET等),靶向治疗在一定程度上改善了这些患者的预后[6],但对于无驱动基因突变的患者而言,治疗获益仍然有限。近年来,免疫治疗逐渐成为无驱动基因突变NSCLC患者的一线治疗标准,尤其是PD-(L)1单药或联合化疗方案,为部分患者带来了生存获益[7],但疗效仍有提升空间,需探索更有效、更耐受的新型治疗方案。
ADC+IO:一线治疗NSCLC的潜在“突破口”
近年来,ADC在肺癌治疗领域取得了重要进展,尤其是在靶点多样性和治疗线数的前移方面——TROP2等靶点的ADC药物不仅在肺癌后线中显示出良好的疗效,还在一线治疗中展现出应用潜力。此外,ADC药物与免疫疗法存在机制上的协同作用:ADC可诱导抗肿瘤免疫反应,这一作用被免疫检查点抑制剂(ICI)进一步增强,从而改善免疫效应功能并提升对肿瘤细胞的识别与杀伤作用[8]。也因此,ADC药物联合免疫治疗有望成为晚期NSCLC一线治疗新突破口。
在今年ASCO年会上,科伦博泰发表了多项对临床决策有重要参考价值的研究结果。其中,TROP2 ADC芦康沙妥珠单抗(sac-TMT)联合PD-L1抑制剂塔戈利单抗一线治疗无驱动基因突变晚期NSLCL的II期临床OptiTROP-Lung01研究公布最新结果,受到行业的广泛关注。
根据ASCO摘要,截至2024年12月30日,该研究共入组81例晚期无驱动基因突变非鳞状NSCLC患者,中位随访17.1个月。确认ORR为59.3%,mDoR为16.5个月,mPFS为15.0个月。各亚组数据显示:
-
在PD-L1 TPS≥50%患者中,ORR提升至77.8%,mPFS为17.8个月;
-
在PD-L1 TPS≥1%患者中,ORR为68.1%,mPFS为17.8个月;
-
在PD-L1 TPS<1%患者中,ORR为47.1%,mPFS为12.4个月。
安全性方面,未发生导致治疗终止或死亡的TRAE。
从现有数据来看,sac-TMT联合塔戈利单抗不仅在晚期野生型非鳞状NSCLC患者中有较强的抗肿瘤活性,且在不同PD-L1表达水平人群中展现出稳定的疗效,显示出治疗人群的广泛性。
竞逐“IO+”联用疗法 sac-TMT优势初显
Sac-TMT并非是唯一入局该适应症领域的TROP2 ADC药物,“IO+ADC”也并不只是科伦博泰一家的探索方向。
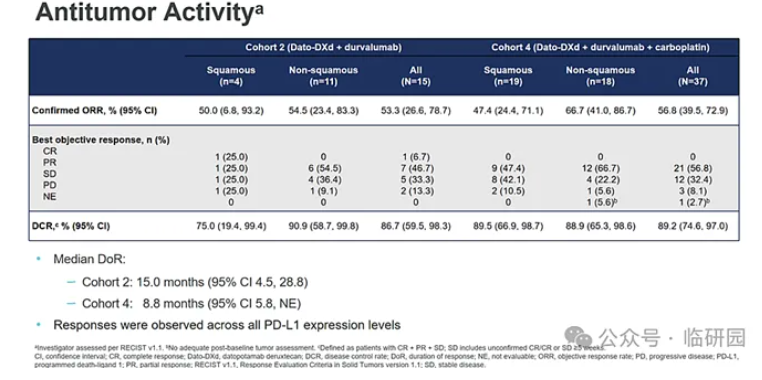
阿斯利康/第一三共也将Dato-dxd作为PD-1的升级搭档,发起了一项PD-L1+Dato-DXd±卡铂一线治疗晚期野生型NSCLC的TROPION-Lung04研究,其队列2和队列4的数据已公布:
-
PD-L1+Dato-DXd治疗组(队列2)的ORR为53.3%,mDOR为15.0个月,mPFS为7.3个月;
-
PD-L1+Dato-DXd+卡铂治疗组(队列4)的ORR为56.8%,mDOR为8.8个月,mPFS为8.7个月。
从亚组分析来看,Dato-DXd两药及三药方案在非鳞癌人群中的ORR分别为54.5%和66.7%,在鳞癌人群的ORR分别为50.0%和47.4%。
而其发起的另一项PD-1+Dato-DXd±化疗一线治疗晚期野生型NSCLC的1b期临床TROPION-Lung02研究,最新数据已在ASCO官网发表。

数据显示:
-
PD-1+Dato-DXd治疗组确认的ORR为55%,mDOR为20.1个月,mPFS为11.2个月;
-
PD-1+Dato-DXd+卡铂治疗组确认的ORR为56 %,mDOR为13.7个月,mPFS为6.8个月。
从亚组分析来看,两药及三药方案在非鳞癌人群中的确认的ORR分别为52%和57%,mPFS分别为11.2个月和10.8个月;在鳞癌人群中确认的ORR分别为67%和50%,mPFS分别为10.2个月和6.7个月。
此外,吉利德也在积极推进TROP2 ADC联合免疫治疗,其开展的II期EVOKE-02研究显示,Trodelvy+PD-1一线治疗mNSCLC的ORR为56%,mDOR尚未达到;在PD-L1TPS≥50%患者中,ORR为66.7%,mPFS为13.1个月,鳞癌和非鳞癌获益一致。
一线晚期野生型NSCLC作为K药最大的市场,不仅吸引了科伦博泰、阿斯利康/第一三共、吉利德入局其中,积极探索“PD-(L)1+Trop2 ADC”的治疗潜力,还催生出其他创新的“IO+”治疗方案,如PD-1/X双抗联合疗法。
前不久,康方生物宣布PD-1/VEGF+化疗头对头对比K药+化疗的III期临床HARMONi-3研究达到PFS主要终点。在此前的II期研究中,依沃西+化疗一线治疗非鳞状NSCLC患者ORR为54.2%,mPFS为13.3个月。
阿斯利康/第一三共也在ASCO官网公布了Dato-DXd+PD-1/TIGIT 双抗一线治疗晚期NSCLC的最新研究数据(TROPION-Lung04队列5):共40例患者接受联合治疗,其中72.5%为非鳞癌,确认的ORR为57.5%,DoR和PFS数据尚不成熟。安全性方面,≥G3 TRAE发生率为60%。

基于当前公开数据,在“PD-(L)1+Trop2 ADC”的联合方案中,sac-TMT相比Dato-DXd和Trodelvy联用PD-(L)1,mPFS和ORR更优且安全性更好,有望成为标准治疗“K药±化疗”的最佳升级迭代方案。若将视野进一步拓展至“IO+”范畴,在关键疗效指标上,sac-TMT在PFS、ORR和安全性方面依然优于现有PD-1/X双抗联合疗法,构建出兼具疗效与差异化优势的治疗路径。
随着“IO+”范式成为一线治疗晚期野生型NSCLC新趋势,作为潜在同类最佳的TROP2 ADC,sac-TMT有望成长为未来ADC联合免疫治疗的基石药物,而其联合治疗探索已初现想象空间,值得长期关注。
总结
作为科伦博泰极具关注度的创新ADC产品,芦康沙妥珠单抗已在今年3月获批治疗晚期EGFR突变非小细胞肺癌,此次联合免疫治疗的研究进一步拓展了其一线治疗野生型NSCLC患者的潜力,芦康沙妥珠单抗在跨PD-L1表达亚组中展现出的疗效一致性,或将弥补现有一线免疫治疗的短板,为更广泛的非小细胞肺癌患者带来治疗选择。
更值得期待的是,在合作方默沙东的主导下,sac-TMT已在海外开展5项NSCLC全球性III期临床研究,全球化进程的提速将助力其成为晚期NSCLC的新一代基石疗法,重塑肺癌的治疗格局。
[1] Bray F, Laversanne M, Sung H, Ferlay J, Siegel RL, Soerjomataram I, Jemal A. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024 May-Jun;74(3):229-263. doi: 10.3322/caac.21834. Epub 2024 Apr 4. PMID: 38572751.
[2] Hendriks L E L, Remon J, Faivre-Finn C, et al. Non-small-cell lung cancer[J]. Nature Reviews Disease Primers, 2024, 10(1): 71.
[3] S R H ,Daniel M ,Chris B .The biology and manag